六十多年以前,一个儿童如果确诊患有急性淋巴细胞白血病,就相当于被宣判死刑。这种情况直到长春碱被发现才出现转机。
1958 年,西安大略大学(University of Western Ontario)的研究人员意外发现马达加斯加长春花(Vinca rosea)的提取物会破坏白细胞,具有治疗儿童白血病的潜力。之后,Charles Beer 博士和 Robert Noble 博士成功分离纯化出了其中的活性化合物,并命名为长春碱(vinblastine)。
 ▲图丨Charles Beer 和 Robert Noble(来源:Canadian Medical Hall of Fame)
▲图丨Charles Beer 和 Robert Noble(来源:Canadian Medical Hall of Fame)
第二年,美国制药巨头礼来公司(Eli Lilly)获得专利并投入商业生产,长春碱很快与其他强效药物联合使用,用于治疗霍奇金淋巴瘤、睾丸癌、乳腺癌和其他形式的癌症,极大地影响了全球数百万癌症患者的生活和治疗。
至今,长春碱仍然是最有用的化疗药物之一,且没有其他替代品。
工业上生产长春碱是先从长春花中提取和纯化得到前体 “文多灵”(vindoline) 和 “长春质碱”(catharanthine),再将此二者通过简单的体外化学偶联和还原以形成长春碱。
然而,这种方式产率极低,一般来说,500 公斤的长春花干叶仅能获得 1g 长春碱。原材料长春花的供应源又仅限于印度、中国等少数国家。这些客观条件使得长春碱的供应本就不稳定,新冠疫情爆发后,弊端暴露无遗,长春花供应短缺致使一些癌症患者被迫中断治疗。
寻找除植物提取外的有效生产途径,实现供应链的多元化,才能从根本上保障长春碱的稳定供应。一项近期发布的重磅研究,让更多癌症患者看到了希望。
2022 年 8 月 31 日,在 Nature 上在线发布了一篇题为“A microbial supply chain for production of the anti-cancer drug vinblastine”的文章,研究人员使用高度工程化的酵母从头合成了抗癌药物长春碱的前体:文多灵和长春质碱。该项研究由合成生物学产业化先驱、美国工程院院士 Jay D. Keasling 团队和丹麦技术大学(DTU)诺和诺德基金会生物可持续性研究中心的 Michael K. Jensen 团队合作共同完成。张杰高级研究员为文章的第一作者。
 (来源:Nature)
(来源:Nature)
“这项研究利用酿酒酵母作为宿主生物,可再生生物质(葡萄糖和色氨酸)作为底物,能够作为完全不受作物种植因素和供应链影响的长春碱新生产途径。”张杰表示。
多达 30 个酶促反应和 56 个基因编辑
据张杰介绍,这是目前已知的从植物转移到微生物的最长的生物合成途径。
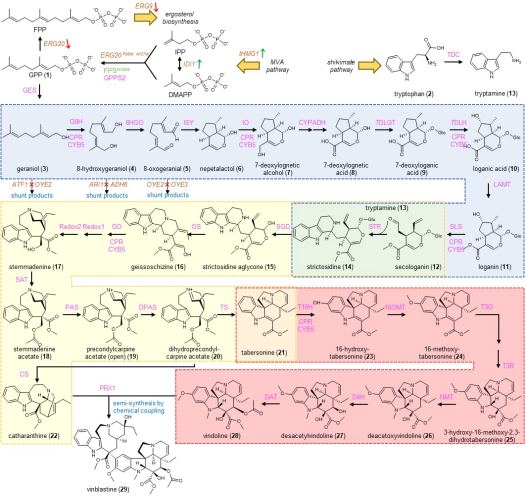
在酿酒酵母中重构的生产途径,包括从酵母天然代谢产物香叶基焦磷酸(geranyl pyrophosphate)和色氨酸(tryptophan)到文多灵和长春质碱的 30 个酶促步骤。构建过程中总共进行了 56 个基因编辑,包括表达来自植物的 34 个异源基因 ,以及删除、敲低和过表达 10 个酵母基因,以改善两种前体“文多灵” 和 “长春质碱”的从头生产和积累。
“从植物到酵母,很多蛋白的活性不能得到完全的转化。其一是很难在酵母中进行表达;其二是表达之后没有相应的活性,这是很大的难点。”张杰告诉生辉 SynBio。
整个途径是相当复杂的。在长春花中,这些参与反应的酶至少分布在 5 个区室中(细胞质、质体、内质网、细胞核和液泡),因此涉及不同组织和细胞类型之间的运输。
为了在酵母中重构长春碱的合成途径,研究人员根据底物和产物的可用性,将长春碱途径分为 3 个模块,分别为:生产中心中间体异胡豆苷的模块,生产它勃宁(Tabersonine)和长春质碱的模块,以及生产文多灵的模块。
 (来源:Nature)
(来源:Nature)
在研究过程中,研究人员将每个模块分别在酵母中表达,以单独测试和确认该部分途径的功能可行性。最终,整合进 3 个模块并优化后的酵母菌株,成功地利用葡萄糖和色氨酸生产得到了文多灵和长春质碱,产量分别为 13.2 μg*L-1 以及 91.4 μg*L-1。研究人员还利用工业生产长春碱的方法,在分别纯化两种前体之后进行偶联,成功合成了长春碱,产量为23.9 μg*L-1。
张杰告诉生辉 SynBio,团队曾尝试在酵母中进行长春碱的全合成,但是没有成功。“目前来看,文献里报道的催化最后一步反应的酶有可能并不是特异性的酶。而且在植物里面最后一步也是非常低效的,能提取到的长春碱是非常非常低的,更多的是文多灵和长春质碱。”
他也表示,未来在酵母里做全合成是有可能的,但是这种全合成形式可能还有其他的阻碍因素。
“长春碱作为一个抗癌的药物,通过阻碍微管的组装从而抑制癌细胞的生长。微管是真核细胞结构里面非常重要的骨架,它的组装带动了细胞的有丝分裂。同理可以推测,长春碱在酵母里合成出来同样会抑制酵母的生长。从生产的角度来讲,有可能生产两个前体分泌出胞外再偶联获得长春碱,恰恰是更可行的方案。”
“我们这项研究显示通过工程化酵母发酵生产文多灵和长春质碱有很大潜力,可以完全或部分取代目前从长春花中提取生产这两个重要前体。”
不过,张杰也严谨地补充道,“长春碱的微生物发酵合成离工业化生产还是有很大距离的,目前仅是一个验证合成生物学可行性的研究,需要进一步放大和优化。首先要解决的就是通量低效的问题,目前得率还是很低的。未来不排除会用其他的酵母来做不同的合成途径。”
历时 8 年,目标是整个单萜吲哚生物碱家族
实际上,此次长春碱的生物合成只是团队第一个公布的成果。“我们瞄准的是整个单萜吲哚生物碱(MIA)家族。”
单萜吲哚生物碱(MIA)是一个多样化的复杂植物次生代谢产物家族,其家族的许多分子具有独特的药用特性,目前已经分离鉴定出来的,在结构和生物活性上差异非常大的有三千多种,这其中就包括抗癌治疗药物长春碱和长春新碱(vincristine)。
单萜吲哚生物碱虽然是小分子,但分子量相对较大立体结构也较复杂,采用化学合成手段获得的异构体难于纯化。而生物合成相对于化学合成特异性更高,在生产这些结构复杂的天然产物方面独具优势。“只要酶是确定的,得到的产物往往也是专一的。”
这整个项目的开始要追溯到 2014 年。这一年,张杰正式成为 Jay Keasling 课题组的一名研究员。而在此之前,酵母的代谢工程研究就一直是张杰的兴趣所在。
2004 年,张杰从浙江大学毕业后前往丹麦留学,硕士、博士均师从代谢工程和模型领域的先驱 Jens Nielsen 教授。博士毕业后,他进入麻省理工化学系 Gregory Stephanopoulos 教授的实验室开展博士后研究。“我的课题一直都是与代谢相关的。”
 ▲图丨张杰(来源:受访者提供)
▲图丨张杰(来源:受访者提供)
2014 年初,丹麦技术大学(DTU)诺和诺德基金会生物可持续性研究中心刚刚成立不久,Jay Keasling 教授正在组建一个开展酵母合成生物学研究的实验室。张杰认为这是一个很好的机会,于是他再次回到了丹麦,加入 Jay Keasling 的课题组,开始利用工程酵母生产一些高附加值的天然产物。
从一开始,张杰就看好利用工程酵母生产植物天然产物尤其是药物的前景,因此选择了单萜吲哚生物碱。
张杰告诉生辉 SynBio,这个项目于 2014 年底立项,2015 年开始推进工作。“并不是从一开始就选定长春碱,因为当时它的合成途径尚不清楚,我们想做的是可用于合成所有单萜吲哚生物碱家族的酵母生产平台。”
2015 年~2018 年,团队主要进行标准元件与合成生物学工具的开发和挖掘,还包括分析化学的方法的建立以及各种平台的技术。前期大量的准备工作很快就迎来了付诸实践的机会。
2018 年,在 Science 上发表的一项研究打通了长春碱完整合成路径,这也意味着研究人员将能够通过合成生物学技术生产长春碱。
“我们对此感到很兴奋,这是验证优化的底盘和开发的工具的好机会,同时我们也清醒地认识到这是一个巨大的挑战,毕竟之前还从来没有人做过这么长的合成途径。于是,我们从 2018 开始推进生物合成长春碱的工作。”
将作为主要合伙人与 Jay Keasling 及 Michael Jensen 成立新公司
“长春碱的合成途径是最长的单萜吲哚生物碱生物合成途径之一,既然可以做这么长、这么复杂的途径,更简单的自然也是可以的。这项研究将工程酵母定位为一个可扩展的平台,其可用于生产 3000 多种天然 MIA 以及几乎无限数量的非天然衍生物。” 张杰说道。
除长春碱外,团队还在推进其他一些 MIA 药物在酵母中合成的研究,包括一些精神类药物和治疗药物成瘾(比如毒瘾和酗酒)的药物。
“我们选择的目标产物一定是市场需求和价值都很可观,且具备创新挑战的药物”,张杰说,“除了推进天然产物的合成,团队也在做一些非天然的化学修饰,通过添加一些其他的基团去改变药物的药动力或者代谢,比如更容易吸收或者让半衰期更长,去做药效更好、毒性更低的新药。”
张杰还透露,他将作为主要合伙人与 Jay Keasling 成立新公司。这也将是 Jay Keasling 以合伙人的身份在丹麦成立的第一家公司。“目前公司正在筹备中,很多工作都已经就绪,将于近期宣布成立。”
“未来,我们将通过这家合成生物学公司来产业化这一平台技术,这是我们接下来的工作重点,或者说是公司的一个工作重点。”
“接下来主要还是找到新的天然产物做合成途径的解析。已知的 3000 多种天然 MIA,绝大多数的合成途径是未知的,像长春碱也是到 2018 年才确定。解析它们的合成途径是一个很重要的工作。”张杰说。
