药融云数据(www.pharnexcloud.com)显示:2022年4月12日,国家药品监督管理局(NMPA)正式批准施维雅(Servier)易安达(通用名:盐酸伊立替康脂质体注射液,Irinotecan Liposome Injection)上市,与5-氟尿嘧啶(5-FU)和亚叶酸(LV)联合用于治疗接受吉西他滨治疗后进展的转移性胰腺癌患者。

药融圈,旗下药融云数据:www.pharnexcloud.com
胰腺癌因其症状隐匿、恶性程度高、致死率高,被称为“癌症之王”。最新国内研究数据显示,胰腺癌五年生存率仍不足10%。根据2020年全球最新癌症负担数据显示,2020年中国胰腺癌新发124994人,死亡121853人。这些患者早期诊断率不足5%,约60%的患者首诊时已转移、约30%的患者首诊时处于局部进展期。目前对于转移性胰腺癌的临床治疗仍以化疗为主,但受制于药物有限且效果不够理想,患者获益比率低。胰腺癌患者面临总体生存期短,生存质量低的巨大挑战。
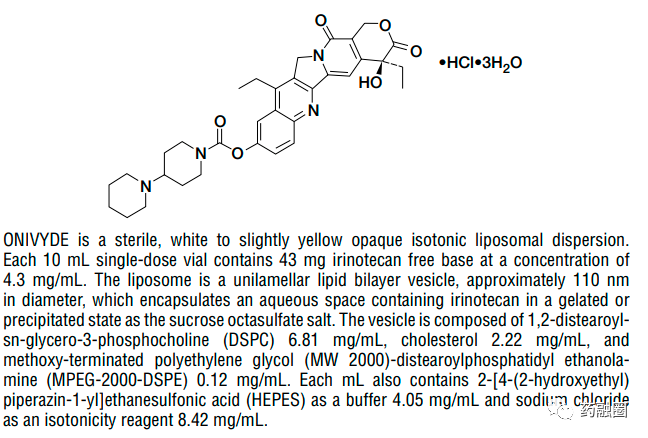
构成ONIVYDE®(盐酸伊立替康脂质体注射液原研英文商品名)的聚乙二醇脂质体是一种含有伊立替康(拓扑异构酶1抑制剂)的双层脂质,被设计用于触及并有效治疗胰腺肿瘤。保护伊立替康不被早期转化为活性代谢物SN-38,这种聚乙二醇脂质体包封有助于伊立替康在体循环中保持更长的时间。这增加了肿瘤内药物的沉积和接触,从而更强有力地抑制肿瘤生长。相关专利:WO-2005107712;于2025年到期。中国专利:CN 108366965 A。
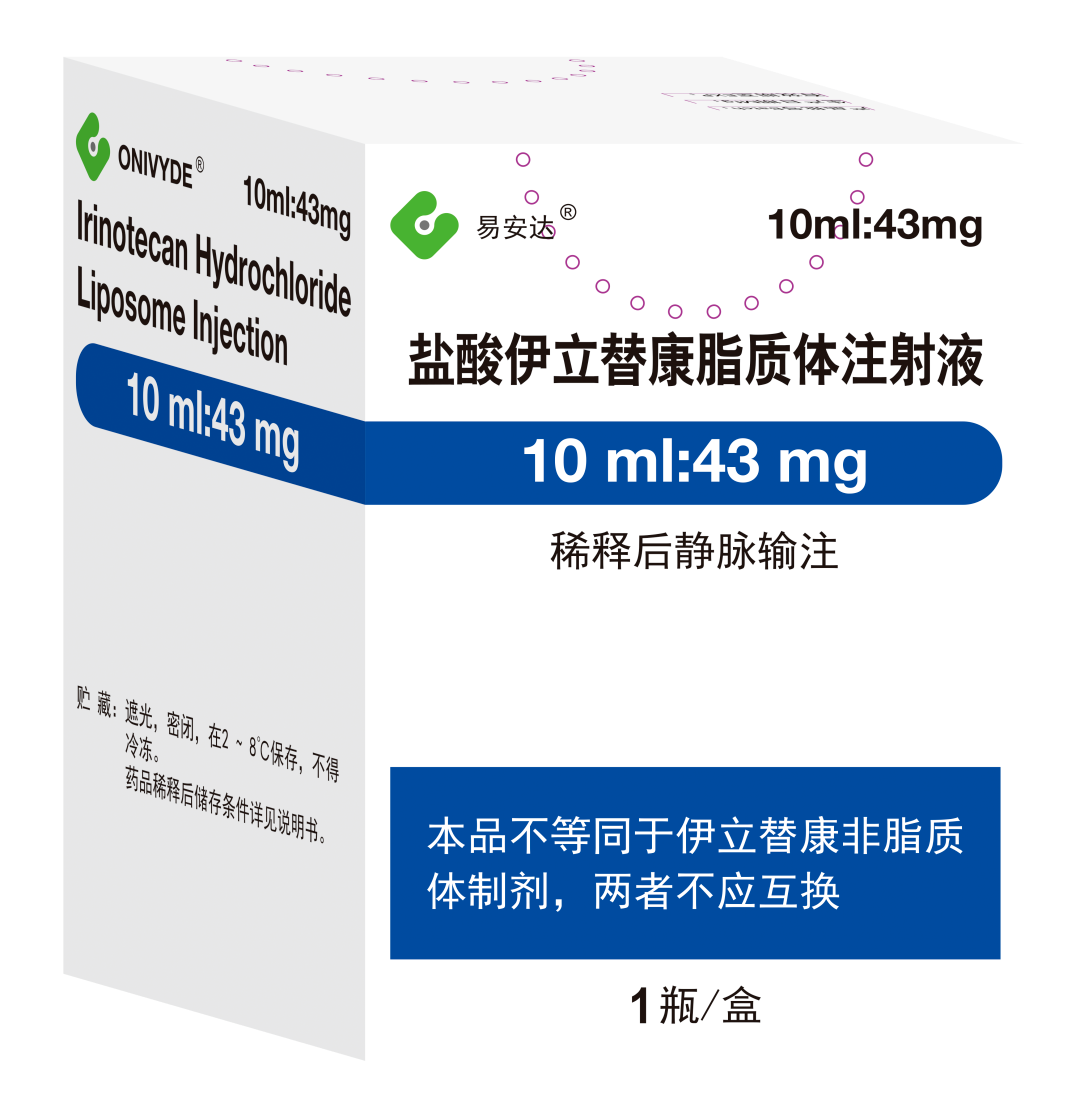
由于伊立替康的化学结构会根据环境pH情况在内酯型和开环型的羧酸盐形态间相互转变,两种形式呈动态平衡。其在酸性条件下为内酯形式,而在生理条件下(pH7.4)会转变为羧酸盐形式。但内酯环却是伊立替康发挥抗肿瘤活性的必需结构,因此开发其脂质体制剂需找寻合适的方法来稳定其结构中的活性部位--内酯环。ONIVYDE®运用了改进的梯度法进行载药,使用蔗糖八硫酸盐使得伊立替康在水相中呈胶凝状或沉淀而被稳定包载。其处方磷脂组成摩尔比为:DSPC:CHOL:DSPE-mPEG2000= 3:2:0.015,药物包封率可达90%以上。最终产品粒径在110nm左右,药脂比高达八百多克伊立替康每摩尔磷脂。
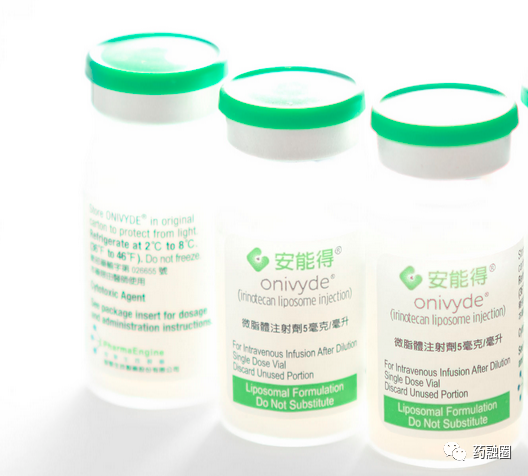
盐酸伊立替康脂质体注射液ONIVYDE®最早由 Academic Medical Center与HERMES BioSciences 开发。
2003年6月,中国台湾省的智擎生技(Pharma Engine)引进其亚洲区域权益(含日本),代号为PEP02。
2005年9月,智擎生技获得欧洲区域权益。
2009年,Merrimack Pharmaceuticals收购HERMES BioSciences 。
2011年5月,智擎生技与美国Merrimack Pharmaceuticals达成PEP02欧洲及亚洲(除中国台湾地区)授权合作。

Merrimack Pharmaceuticals于2014年9月将ONIVYDE®(MM-398)在美国及中国台湾以外的区域专属授权给予美国Baxter公司(NYSE: BAX),后来于2015年分割为Baxalta公司(NYSE: BALT)。之后,Shire公司(LSE: SHP, NASDQ: SHPG)于2017年6月并购Baxalta公司,后续并将ONIVYDE®出售予法国Servier公司。2017年4月Merrimack公司再将其所拥有ONIVYDE®与美洲之所有权利售予法国Ipsen公司(ENXTPA: IPN)。因此,现今致力于ONIVYDE®的开发有智擎生技公司(中国台湾)、 Servier公司(欧洲及亚洲区)及Ipsen公司(美洲区)。
2018财年,盐酸伊立替康脂质体注射液ONIVYDE®销售额约为1.24亿美元。IPSEN(美洲区),盐酸伊立替康脂质体注射液ONIVYDE®,2019年该药品销售额约1.35亿欧元,2020年业绩1.23亿欧元。(非全球总销售额)
本品原研在开发的适应症有:一线晚期胰腺癌治疗;与托泊替康比较治疗铂类一线进展小细胞肺癌3期临床研究;小细胞肺癌二线治疗2/3期临床研究等等。
本款高难度制剂(NDDS,新型药物递送系统):绿叶制药、石药集团、恒瑞医药、上海医药/沈阳药科大学(2016年及以前申报的还有科伦药业、海正药业、齐鲁制药)等等在布局。
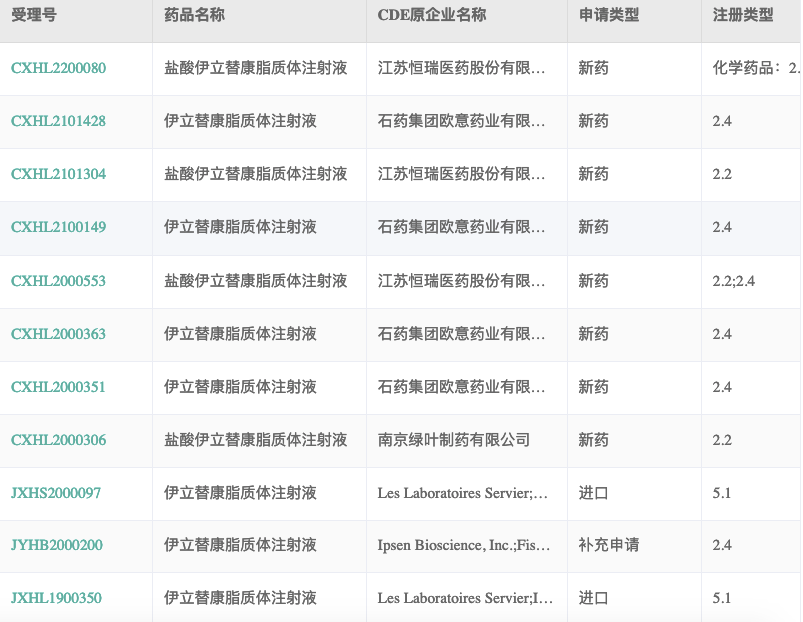
2022年4月20日,药融圈数据(www.pharnexcloud.com)显示,恒瑞医药研发的盐酸伊立替康脂质体注射液已经向NMPA递交上市申请,基于开展的HR-IRI-APC3期临床。
近期,石药集团欧意药业有限公司的伊立替康脂质体注射液上市申请(CYHS2200667)亦递交。
此外,由于技术门槛以及一定程度上know-how的共性,目前布局做脂质体药物的公司,也同时在布局脂质纳米颗粒(LNP)等新型递送药物(如:mRNA疫苗)。
此文仅用于向医疗卫生专业人士提供科学信息,不代表平台立场参考:
NMPA/CDE;
药融云数据:www.pharnexcloud.com;
FDA/EMA/PMDA;
相关公司公开披露;
2022年04月15日药品批准证明文件待领取信息发布,
https://www.nmpa.gov.cn/zwfw/sdxx/sdxxyp/yppjfb/20220415094455198.html;
《中华医学会肿瘤学分会胰腺癌早诊早治专家共识》(2020);
World Heaith Organization, Globocan 2020 for pancreas. https://gco.iarc.fr/today/data/factsheets/cancers/13-Pancreas-fact-sheet.pdf;
https://www.onivyde.com/hcp/;
http://www.pharmaengine.com/zh-hant/;
ONIVYDE®盐酸伊立替康脂质体注射液,美国:https://yaorongyun-source.oss-cn-shanghai.aliyuncs.com/FDA/337fb8c54ace476e4be6624ed512d115_207793lbl.pdf;
说明书:https://www.onivyde.com/websites/onivyde_us_online/wp-content/uploads/sites/2/2018/12/14110723/ONIVYDE_USPI.pdf;等等。
